“溶石先锋”
工程化布拉氏酵母菌的无创胃结石疗法
Non-invasive gastric calculus therapy with engineered Saccharomyces boulardii
胃结石(Gastric Bezoars)
胃结石是指在胃内形成的难以消化的凝固物或异物团块,根据其成分主要分为植物性胃结石(由柿子、山楂、黑枣等富含鞣酸的食物形成)、毛发性胃结石(由吞食毛发形成)以及药物性胃结石等类型。其中,植物性胃结石在临床上最为常见。在中国,胃结石的发病率约为0.4%,每年有数以万计的患者正在经历它的折磨。患者通常表现为上腹部疼痛、饱胀、恶心、呕吐等症状,严重者可继发胃溃疡、胃出血甚至胃穿孔,对患者生活质量造成显著影响[1,2]。
现有治疗及其局限性
药物溶石
临床上常用口服碳酸氢钠或纤维素酶制剂,在胃酸环境中易失活,且单次给药后难以在结石局部维持有效药物浓度,往往需要多次、长期服药,治疗效果不稳定,对于较大的结石效果欠佳。

内镜下碎石
内镜下碎石(如圈套器切割、激光碎石等)是目前常用的一线干预手段,但其属于侵入性操作,对设备和操作者技术要求高,患者体验不佳,且存在胃黏膜损伤、出血甚至穿孔的风险,对于巨大的结石往往需要多次操作才能完全清除。
外科手术取石
对于药物和内镜治疗失败的病例,外科手术成为最后的选择。但手术创伤大、恢复周期长,且存在术后并发症风险,对患者身体机能影响较大。
新方法
为解决传统胃结石治疗方法的局限性,我们提出一种新型的治疗方案
我们拟构建一种靶向降解胃结石的新型工程布拉氏酵母菌。该菌株通过表面展示胃黏膜黏附因子,实现对胃壁的特异性定植,为持续发挥治疗作用提供保障。治疗模块整合了可协同降解果胶与纤维素的复合酶系,能够从结构层面逐步瓦解植物性结石的骨架,实现高效溶解。为保障生物安全,菌株引入了双重环境响应调控机制:一方面构建营养缺陷型,使其在自然环境中无法存活;另一方面设计基于胃内酸性环境与人体体温的逻辑门控制系统,确保菌株仅在胃内发挥功能,离体后迅速失活。该工程菌集靶向定植、酶解治疗与可控自限性于一体,为胃结石提供了一种高效、无创且安全的生物治疗新策略,具有明确的临床转化潜力。
基因线路设计
黏附模块
治疗模块
双重安全模块

黏附模块
底盘菌选择:我们最终选择布拉氏酵母菌CNCM I-745作为底盘菌。该菌株具有多项理想特性:胃酸环境中存活率高达75%,最适生长温度37℃完美匹配人体,且作为药用酵母,不会在肠道永久定植,安全性明确。更重要的是,它已有成功改造的先例,遗传操作可行。在此基础上,我们进一步敲除了其内源URA3基因,构建尿嘧啶营养缺陷型菌株,为后续多轮整合提供高效的筛选平台[3]。
为了让工程菌能在胃里“住下来”,我们借鉴了自然界最成功的胃部定植者——幽门螺杆菌的策略。我们截取了其黏附蛋白BabA中最小的功能性片段C51,该片段专门识别胃壁的主要成分——胃黏蛋白MUC5AC上的Lewis b抗原。
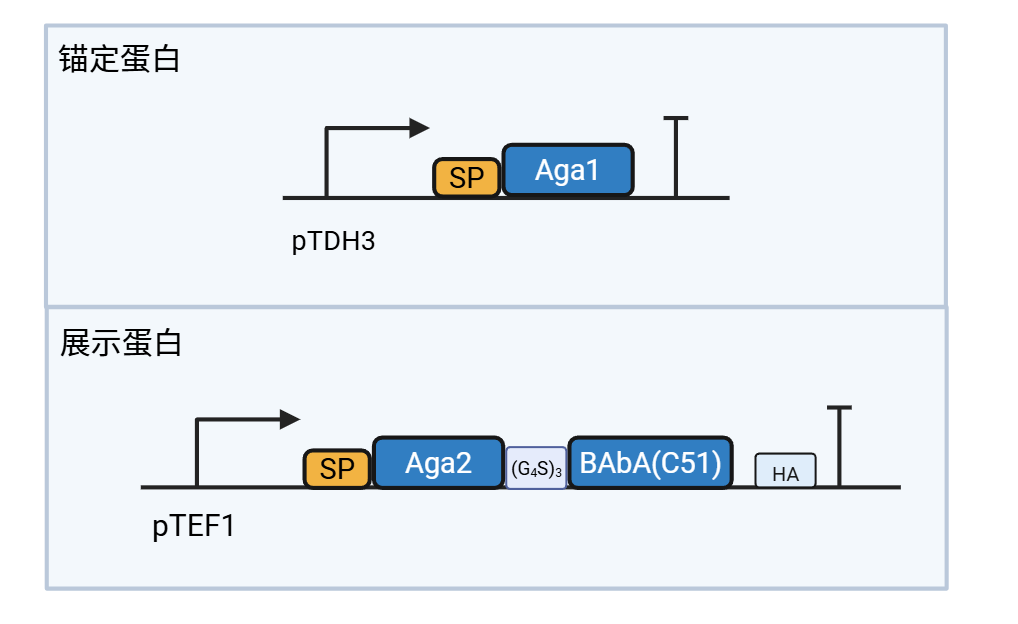
如何将这个片段安全地安装到我们的益生菌上?我们利用了已在布拉氏酵母菌中验证成熟的Aga1-Aga2表面展示系统,将C51高效地展示在酵母细胞壁的最外层。这样一来,我们的工程菌就获得了精准锚定于胃黏膜的能力,为后续持续分泌溶解酶、彻底清除胃结石,争取了足够的作用时间[4]。
我们的表达盒包含两个独立的转录单元:转录单元1 高效驱动锚定蛋白 AGA1 的表达;转录单元2 则表达一个融合蛋白,由 α-factor信号肽、展示蛋白 Aga2、柔性连接肽 (G₄S)₃ 以及黏附功能域 BabA(C51) 组成。α-factor信号肽是酵母中最经典的分泌信号,负责引导整个融合蛋白进入分泌途径,最终将C51展示在细胞壁表面;Aga2作为展示支架,通过连接肽确保C51能够自由伸展、有效结合靶点[5-7]。
构建时,我们先将该表达盒在大肠杆菌中进行扩增和组装,再利用 CRISPR-Cas9 技术将其精准整合到布拉氏酵母菌的染色体XI-3中,从而完成黏附模块的构建。
治疗模块
治疗模块包含四个独立的转录单元,分别由四种不同的强启动子——PGK1、TEF1、TDH3、ADH1驱动。采用不同的启动子可有效避免同源序列引发的重组丢失,确保多基因系统的长期遗传稳定性。每个转录单元均融合表达了酵母经典的α-factor信号肽,引导酶蛋白进入分泌途径,实现从细胞内向胞外的高效运输。
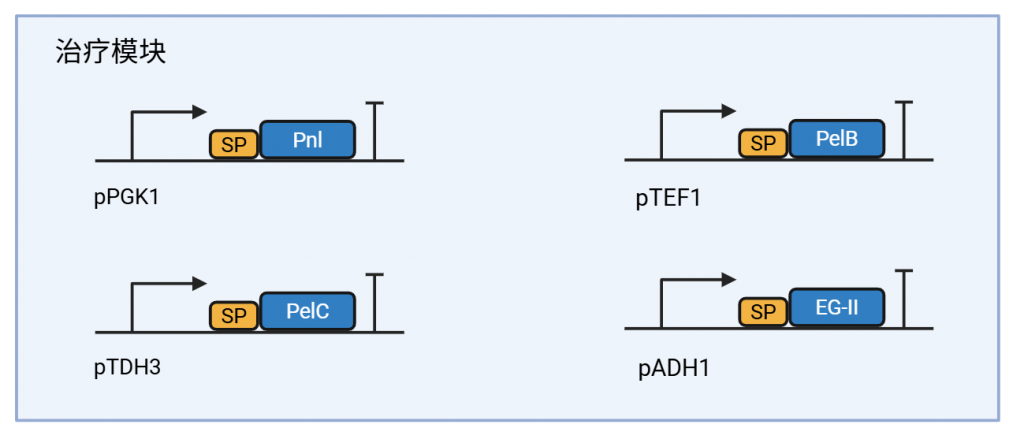
三个果胶酶基因均来自同一细菌,彼此协同,构成完整的果胶裂解系统:
Pnl(果胶裂解酶)特异性切割果胶分子中高度甲酯化的区域。植物性胃结石中的果胶恰恰以高甲酯化形式存在,因此Pnl是瓦解结石核心结构的“主攻手”。
PelB(果胶酸裂解酶B):倾向于切割甲酯化与未甲酯化区域的交界处,充当“开路先锋”。它在Pnl切割后或复杂果胶网络中开辟新的作用位点,为后续酶分子提供攻击入口。
PelC(果胶酸裂解酶C):高效切割未甲酯化的多聚半乳糖醛酸区域,以外切方式从分子末端或切口处逐步“咬下”寡糖片段。它与Pnl、PelB协同作用,确保果胶大分子被彻底分解为可溶小分子,实现对结石的彻底瓦解。
三者构成的裂解系统,要比单一酶更加高效,是因为果胶本身是一个非常复杂的分子,单一酶无法高效地将其彻底瓦解,而基因来自细菌,使用前必须经过密码子优化[8]。
纤维素酶EG-II(内切葡聚糖酶II) 来源于工业纤维素酶生产菌株里氏木霉,是该菌株纤维素酶系中的核心内切酶之一。EG-II通过随机切割纤维素链内部的β-1,4-糖苷键,高效瓦解植物细胞壁的纤维素骨架[9]。
四个单元构成完整表达盒,最后利用CRISPER-Cas9整合于布拉氏酵母菌染色体XII-5。
双重安全模块
1.敲除布拉氏菌的THI6 基因,使菌株依赖硫胺素(维生素B1):
我们通过敲除布拉氏酵母菌的THI6基因,使其成为硫胺素(维生素B1)营养缺陷型菌株。该菌株仅在硫胺素浓度高于1 ng/mL的环境中才能存活。研究表明,人体肠道内硫胺素浓度约为1–10 ng/mL,胃内浓度虽略低,但实验证实仍足以支持其存活;而自然水体、土壤等环境中硫胺素浓度远低于该阈值。这一设计确保了工程菌在人体胃肠道内可正常发挥治疗功能,一旦被排出体外,则无法在自然环境中存活或增殖,实现了精准治疗与生物安全的双重保障[10]。
2.低pH诱导型启动子驱动毒素基因:
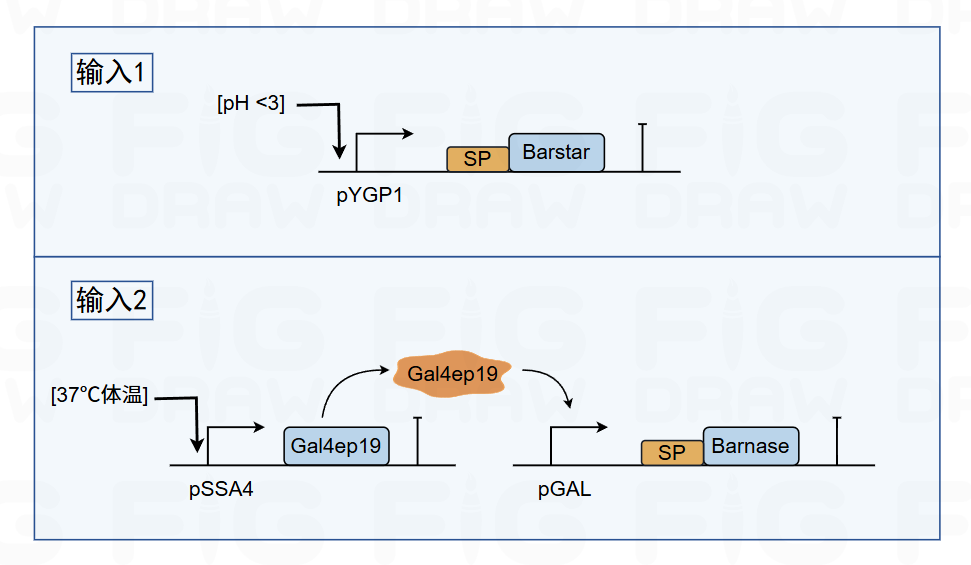
安全模块采用双输入与门设计,确保工程菌仅在胃内环境中存活。
第一个输入信号:pH ≤ 3。我们使用经过工程化改造的 YGP1启动子,该启动子仅在 pH ≤ 3 时被强烈激活,驱动 Barstar抗毒素表达。Barstar 是 Barnase 毒素的特异性抑制剂,通过空间位阻阻断其活性位点[11]。
第二个输入信号:37℃体温。 我们引入了一个经文献证实的双温度敏感放大系统:在 37℃ 时,热激启动子 P_SSA4 驱动冷敏感转录因子 Gal4ep19 表达,进而激活 GAL启动子,高效驱动 Barnase毒素 的表达[12,13]。
只有当低pH和37℃两个信号同时存在时,抗毒素与毒素共同表达并相互中和,细胞得以存活。一旦离开胃(pH升高)或排出体外(温度降低),抗毒素信号消失,而毒素仍在肠道中表达,或在环境中因营养缺陷型屏障而无法存活。
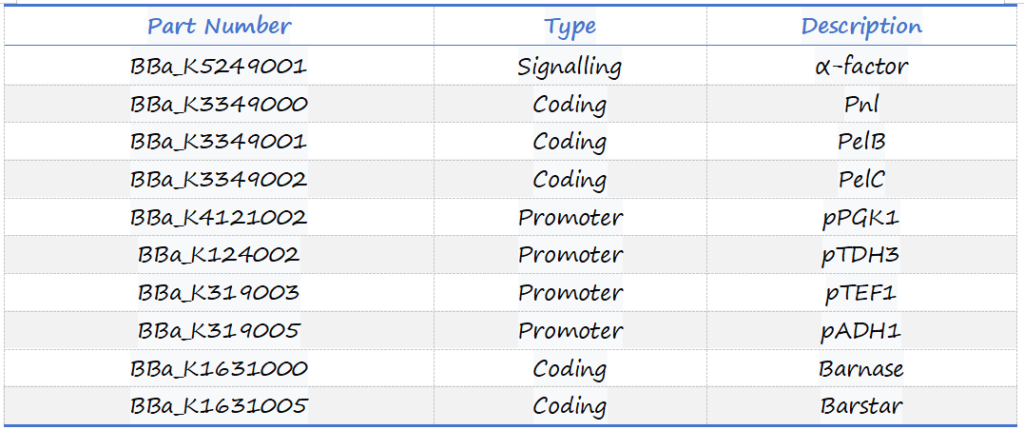
元件
参考文献:
[1]Rong SU,Ruirui HOU,Xiangkun MENG,Yu MIAO,Feixiong ZHANG,Jigang RUAN,Shaoqi. YANG. Comparative analysis of endoscopic treatment and conservative treatment in 197 cases of gastric stones[J]. The Journal of Practical Medicine, 2024, 40(10): 1389-1395.
[2]Ladas SD, Kamberoglou D, Karamanolis G, Vlachogiannakos J, Zouboulis-Vafiadis I. Systematic review: Coca-Cola can effectively dissolve gastric phytobezoars as a first-line treatment. Aliment Pharmacol Ther. 2013 Jan;37(2):169-73. doi: 10.1111/apt.12141. PMID: 23252775.
[3]Pais P, Almeida V, Yılmaz M, Teixeira MC. Saccharomyces boulardii: What Makes It Tick as Successful Probiotic?. J Fungi (Basel). 2020;6(2):78. Published 2020 Jun 4. doi:10.3390/jof6020078
[4]Waldrip ZJ, Burdine L, Peterson EC, Rainwater RR, Min Y, Burdine MS. A functional surface display system in Saccharomyces boulardii for protein absorption in simulated intestinal fluids. iScience. 2025 Aug 6;28(9):113303. doi: 10.1016/j.isci.2025.113303. PMID: 40894886; PMCID: PMC12390945.
[5]Yang H, Wang L, Zhang M, Hu B. The Role of Adhesion in Helicobacter pylori Persistent Colonization. Curr Microbiol. 2023 Apr 18;80(5):185. doi: 10.1007/s00284-023-03264-6. PMID: 37071212
[6]Ansari S, Yamaoka Y. Helicobacter pylori BabA in adaptation for gastric colonization. World J Gastroenterol. 2017 Jun 21;23(23):4158-4169. doi: 10.3748/wjg.v23.i23.4158. PMID: 28694656; PMCID: PMC5483490.
[7]Waldrip ZJ, Burdine L, Peterson EC, Rainwater RR, Min Y, Burdine MS. A functional surface display system in Saccharomyces boulardii for protein absorption in simulated intestinal fluids. iScience. 2025 Aug 6;28(9):113303. doi: 10.1016/j.isci.2025.113303. PMID: 40894886; PMCID: PMC12390945.
[8]Safety evaluation of an extension of use of the food enzyme containing cellulase, endo-1,3(4)-β-glucanase and endo-1,4-β-xylanase from the non-genetically modified Trichoderma reesei strain AR-256. EFSA J. 2024 Jan 8;22(1):e8510. doi: 10.2903/j.efsa.2024.8510. PMID: 38196995; PMCID: PMC10772850.
[9]Safety evaluation of the food enzyme cellulase from the genetically modified Aspergillus niger strain NZYM-EN. EFSA J. 2025 Oct 30;23(10):e9723. doi: 10.2903/j.efsa.2025.9723. PMID: 41180301; PMCID: PMC12572824.
[10]Hedin KA, Kruse V, Vazquez-Uribe R, Sommer MOA. Biocontainment strategies for in vivo applications of Saccharomyces boulardii. Front Bioeng Biotechnol. 2023 Feb 20;11:1136095. doi: 10.3389/fbioe.2023.1136095. PMID: 36890914; PMCID: PMC9986445.
[11]Mireau H, Arnal N, Fox TD. Expression of Barstar as a selectable marker in yeast mitochondria. Mol Genet Genomics. 2003 Oct;270(1):1-8. doi: 10.1007/s00438-003-0879-2. Epub 2003 Aug 19. PMID: 12928865.
[12]Rajkumar AS, Liu G, Bergenholm D, Arsovska D, Kristensen M, Nielsen J, Jensen MK, Keasling JD. Engineering of synthetic, stress-responsive yeast promoters. Nucleic Acids Res. 2016 Sep 30;44(17):e136. doi: 10.1093/nar/gkw553. Epub 2016 Jun 20. PMID: 27325743; PMCID: PMC5041464.
[13]Jiaxi Lin, Zhen Yao, Xiaomei Lyu, Lidan Ye, Hongwei Yu. Development of a dual temperature control system for isoprene biosynthesis in Saccharomyces cerevisiae. Front. Chem. Sci. Eng., 2022, 16(7): 1079-1089 DOI:10.1007/s11705-021-2088-0
